„Hot Paper“ in Angewandte Chemie: Im Käfig zum Wirkort
Wie transportiert man einen hochwirksamen Wirkstoff genau an den Ort, wo er im Körper wirken soll? Chemiker des DWI – Leibniz-Institut für Interaktive Materialien stellen zusammen mit Kollegen der Heinrich-Heine-Universität Düsseldorf (HHU) in der Zeitschrift Angewandte Chemie einen Lösungsansatz dafür vor. Die Idee: Die Verwendung eines Molekülkäfigs, der sich bei Ultraschallbestrahlung öffnet.
In der supramolekularen Chemie werden Moleküle zu größeren, übergeordneten Strukturen zusammengesetzt. Bei geeigneter Wahl der Teilkomponenten setzen sich solche Systeme selbst aus ihren einzelnen Bausteinen zusammen, man spricht dann von Selbstassemblierung.
Bestimmte supramolekulare Verbindungen eignen sich gut als sogenannte Wirt-Gast-Systeme. In solchen Fällen umgibt eine Wirtsstruktur ein Gastmolekül, welches es von der Umgebung abschirmen, schützen und transportieren kann. Dies ist ein Spezialgebiet von Dr. Bernd M. Schmidt und seiner Arbeitsgruppe am Institut für Organische Chemie und Makromolekulare Chemie der HHU in Düsseldorf.
Die Düsseldorfer Chemiker suchten zusammen mit Kollegen vom DWI – Leibniz-Institut für Interaktive Materialien nach einem System, das Wirkstoffmoleküle später vielleicht sogar durch den menschlichen Körper transportieren und vor allem die Fracht an einer gewünschten Stelle freigeben kann.
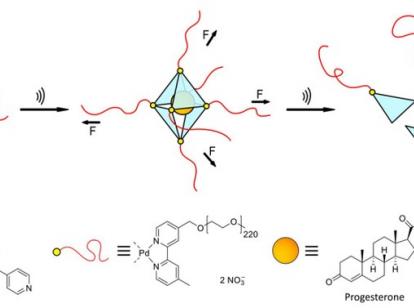
Die Lösungen können diskrete „Pd6(TPT)4-Käfige“ sein: Oktaeder-förmige Strukturen aus vier dreieckigen Paneelen, an deren sechs Ecken jeweils ein großes organisches Molekül sitzt, genauer gesagt ein Palladiumatom, über welches eine lange Polymerkette gebunden ist. Diese Palladiumatome bilden sogenannte koordinative Metallbindungen zu den Paneelen aus, deren Ecken sie anstoßen.
Gibt man die einzelnen Bausteine in richtigem Verhältnis in eine wässrige Lösung, so entstehen die Käfige von selbst. Fügt man anschließend kleinere, hydrophobe Moleküle hinzu, wandern diese in genau bekannter Zahl in die Käfige hinein. Die Forscher haben dies mit den Wirkstoffmolekülen Ibuprofen (Schmerzmittel) und Progesteron (Gelbkörperhormon) gezeigt.
„Der besondere Clou bei unserem System sind die eingebauten Sollbruchstellen“, so Dr. Schmidt, Letztautor der Studie. „Die Palladiumatome verbinden alle Bausteine vergleichsweise schwach. Wenn man es schafft, diese aus dem Verbund zu zerren, bricht das ganze Oktaeder auseinander“, erläutert er.
„Gezerrt“ wird in diesem Fall in Aachen – und zwar mit leistungsstarken Ultraschallquellen, wie sie in der Medizin beispielsweise zur Zertrümmerung von Nierensteinen verwendet werden. Der Ultraschall erzeugt im Wasser Kavitationsblasen. Diese zerplatzen und üben dadurch sehr große mechanische Scherkräfte auf die langen Ketten aus. Die Kräfte sind so stark, dass sie die Palladiumatome buchstäblich aus den Ecken reißen und somit den Oktaederkäfig zerlegen. Die kleinen Wirkstoffmoleküle werden dabei zwar herumgewirbelt, allerdings nicht beschädigt.
„Durch lokale Ultraschallbestrahlung des zu behandelnden Gewebes ließe sich später erreichen, dass der im Käfig transportierte Wirkstoff genau dort freigesetzt wird, wo er zur Therapie benötigt wird“, erklärt Dr. Robert Göstl, Experte auf dem Feld der Polymer Mechanochemie aus Aachen. Dabei dienen die in der Studie eingesetzten Wirkstoffmoleküle nur als Test. Grundsätzlich ist es möglich, dass sehr viele verschiedene, hydrophobe Moleküle in den Käfig gepackt werden. Und es ist – im Gegensatz zu anderen beschriebenen Wirt-Gast-Systemen – nicht notwendig, die Wirkstoffmoleküle chemisch anzupassen, damit sie in den Käfig gelangen. „Für die Behandlung von Krebs wäre zum Beispiel eine Beladung mit Zytostatika denkbar. Indem sie direkt bei einem soliden Tumor freigesetzt werden, könnte vielleicht eine Chemotherapie mit deutlich weniger Wirkstoff und damit mit geringeren Nebenwirkungen durchgeführt werden“, wünscht sich Bernd M. Schmidt.
Hinzukommt, dass sich aufgrund der definierten Beladungsmenge auch genau bemessen lässt, wie viel Wirkstoff am Einsatzort freigesetzt wird. „Die verabreichte Dosis könnte somit sogar präzise berechnet werden“, so Bernd M. Schmidt.
Bei der Studie handelt es sich um einen sogenannten „Proof of Concept“, das heißt, die Machbarkeit des Ansatzes wurde gezeigt. Dies überzeugte auch die Gutachter und Verleger der Zeitschrift „Angewandte Chemie“, die die Veröffentlichung als besonders bedeutsam ansahen. Es ist als „Hot Paper“ eingestuft worden und zur Titelgeschichte der nächsten Zeitschriftenausgabe gemacht worden.
„Nächster Schritt sind Versuche, in denen wir überprüfen möchten, wie menschliche Zellen auf unsere Käfige reagieren. Dies ist notwendig, da vor einem möglichen medizinischen Einsatz sichergestellt sein muss, dass sie nicht toxisch auf die Zellen wirken“, erklärt Bernd M. Schmidt.